再生医療等製品の製造や細胞加工施設の運営において、もっとも頭を悩ませる課題のひとつが適切な設備の導入ではないでしょうか。厳格なGCTP/GMP省令への適合はもちろん、効率的な運用とコストパフォーマンスの両立は、プロジェクトの成否を分ける重要な要素です。
本記事では、新規施設の立ち上げや既存設備の更新を検討されている担当者様に向けて、失敗しないための「設備選定ガイド」をお届けします。規制要件を満たしつつ、現場の運用に即した最適な機器を選ぶための具体的な基準とプロセスを、専門的な視点からわかりやすく解説してまいります。ぜひ、貴社の設備計画にお役立てください。
再生医療における設備選定の結論:GCTP適合とリスクベースアプローチが鍵

再生医療における設備選定は、単に高機能な機器を購入することではありません。もっとも重要なのは、その設備がGCTP(再生医療等製品の製造管理及び品質管理の基準)などの規制要件に適合し、かつリスクベースアプローチに基づいて管理可能であるかという点です。ここでは、選定の根幹となる4つの視点について解説します。
GCTP/GMP省令が求める構造設備要件の理解
再生医療等製品の製造所には、製品の品質を確保するために必要な構造設備が求められます。GCTP省令やGMP省令では、製造工程における人為的な誤りを最小限にし、製品の汚染や品質低下を防ぐためのハードウェア要件が規定されています。
設備選定においては、以下の点がクリアされているかをまず確認しましょう。
- 清浄度管理: 作業内容に応じた清浄度区域(グレードA〜D)に設置可能か
- 材質の適切性: 錆びや発塵がなく、消毒剤に耐えうる材質か
- メンテナンス性: 点検や清掃が容易な構造か
これらの要件を満たさない設備は、いかに高性能であっても規制対応の観点から導入リスクが高くなります。
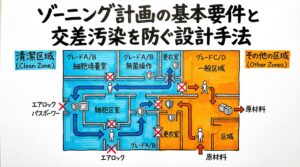
クロスコンタミネーション(交叉汚染)の防止機能
細胞培養において最大の脅威であるクロスコンタミネーション(交叉汚染)や微生物汚染を防ぐ機能は、設備選定の最優先事項といえます。特に、複数の患者様の細胞を同時に扱う施設では、検体取り違えやウイルス等の拡散防止が生命線となります。
具体的には、以下のような機能が求められます。
- 気流制御: 安全キャビネット等の適切な給排気バランスとエアロゾル封じ込め
- 閉鎖系システム: 開放系操作を減らし、外気との接触を断つ構造
- ワンウェイ動線: 作業者や物品の動線を考慮した機器配置とパスボックスの活用
汚染リスクをハードウェア側でどこまで低減できるかが、安定運用の鍵を握ります。
バリデーション(適格性評価)実施の容易性
どれほど優れた設備でも、その性能が恒常的に発揮されていることを科学的に証明できなければ、再生医療の現場では使用できません。これがバリデーション(適格性評価)です。設備を選定する際は、「バリデーションが実施しやすいか」という視点を持つことが大切です。
- IQ/OQ対応: メーカーからIQ(据付時適格性評価)やOQ(運転時適格性評価)の実施要領書やサポートが提供されるか
- 校正ポート: 温度やCO2濃度などのセンサー校正が容易に行える測定孔があるか
- ドキュメント: 材質証明書や校正証明書などの必要書類が完備されているか
バリデーションの工数を削減し、スムーズに運用開始できる機種を選ぶことが、プロジェクト全体の効率化につながります。
データインテグリティ(DI)対応の必要性
近年、規制当局の査察において重要視されているのがデータインテグリティ(DI:データの完全性)です。製造や品質管理に関わるデータが、生成から保存まで改ざんされることなく、正確に維持されていることが求められます。
設備選定においては、以下の機能を持つ機器が推奨されます。
- アクセス管理: IDとパスワードによるユーザー権限の設定
- 監査証跡(オーディットトレイル): 「いつ・誰が・何をしたか」の操作ログ自動記録
- データバックアップ: データの安全な保存と復旧機能
特にPC制御を行う分析機器や培養装置では、DI対応が不十分だと指摘事項となる可能性が高いため、慎重な確認が必要です。
失敗しない設備選定に不可欠な3つの判断基準

数あるメーカーや機種の中から自社に最適な一台を選ぶには、明確な判断軸が必要です。カタログスペック上の数値だけでなく、実際の運用シーンを想定した「使い勝手」や「将来性」を考慮することで、導入後の後悔を防ぐことができます。ここでは、特に重視すべき3つの基準をご紹介します。
清掃・消毒・滅菌のしやすさ(サニタリー性)
CPC(細胞培養加工施設)内では、日常的な清掃と定期的な除染作業が欠かせません。そのため、設備の形状や材質が「サニタリー性(衛生的であること)」に優れているかは極めて重要な判断基準です。
チェックすべきポイントは以下の通りです。
- 凹凸の少なさ: ほこりや汚れが溜まりにくいフラットなデザインか
- コーナーのR加工: 隅々まで拭き取りやすいよう、角が丸く加工されているか
- 耐薬品性: アルコールや次亜塩素酸ナトリウム、過酢酸などの消毒剤で劣化しないか
清掃に時間がかかる設備は、作業者の負担増だけでなく、汚染リスクの増大にもつながります。日々のケアが容易な設計を選ぶことが、長期的な品質維持に貢献します。
製造プロセスとの整合性とスケールアップへの対応
設備は現在の製造プロセスに合致しているだけでなく、将来的な生産計画にも対応できるものであるべきです。研究開発段階から治験、そして商用生産へとフェーズが進むにつれて、処理量や求められる管理レベルは変化します。
- スケーラビリティ: 小規模機から大規模機へのスケールアップ時に、データの相関性が取れるか
- 自動化への拡張性: 将来的に自動培養装置などとの連携が可能か
- 設置スペース: 増設を見越したサイズ感やスタッキング(積み重ね)の可否
現状のニーズだけで判断せず、3年後、5年後の事業計画を見据えた「拡張性のある選択」を心がけましょう。
メーカーによる保守点検・校正サポート体制
再生医療の製造は24時間365日止まることが許されないケースが多く、設備のダウンタイムは甚大な損失をもたらします。そのため、製品そのものの性能以上に、メーカーや代理店のサポート体制が重要になります。
| 確認項目 | チェックポイント |
|---|---|
| 緊急対応 | 故障時に即日または翌日にエンジニアが駆けつけてくれるか |
| 代替機手配 | 修理期間中に代替機を貸し出してくれるか |
| 定期点検 | 年次点検やバリデーション支援のメニューが充実しているか |
| 部品供給 | 消耗品や交換部品の国内在庫は十分か(特に海外製の場合) |
購入価格が安くても、アフターサポートが脆弱であれば、結果的にコストが高くつく可能性があります。信頼できるパートナーとしてのメーカー選びを推奨します。
CPC(細胞培養加工施設)構築における主要設備の選定ポイント

CPCを構築する際には、多くの種類の機器を選定する必要があります。それぞれの機器には特有の選定ポイントがあり、用途に応じた最適な仕様を見極めることが大切です。ここでは、主要な6つの設備について、プロフェッショナルな視点から選定の勘所を解説します。
安全キャビネット・クリーンベンチの選定と気流管理
無菌操作の要となる安全キャビネットやクリーンベンチは、作業者と製品を守るバリアです。選定においては、JIS規格(JIS K 3800等)への適合はもちろん、気流の安定性が重要です。
- DCモーター採用機: 省エネかつ発熱が少なく、室温上昇を抑えられるため推奨されます。
- 気流バランス: 前面シャッターの開度に関わらず、吸気と排気のバランスを一定に保つ機能があるか確認しましょう。
- 清掃性: ワークエリアが一体成型で継ぎ目がないものや、前面ガラスが大きく開いて清掃しやすいものが衛生的です。
細胞製品の場合は、コンタミネーション防止の観点から、循環型のクラスIIタイプA2などが一般的に選ばれます。
CO2インキュベーター(細胞培養装置)の汚染防止機能
細胞にとっての「家」であるCO2インキュベーターは、もっとも汚染リスクに晒されやすい機器のひとつです。培養環境の安定性とともに、汚染防御機能を重視して選定します。
- 滅菌・除染機能: 乾熱滅菌(160℃〜180℃)やH2O2(過酸化水素)除染機能があると、万が一の汚染時や定期メンテナンス時のリセットが確実です。
- 内箱の材質: 抗菌作用のある銅合金製や、清掃しやすいステンレス製が主流です。
- センサー: CO2センサーはIR(赤外線)式が湿度や温度の影響を受けにくく、安定しています。
コンタミネーション発生時のリカバリーにかかる手間を考慮し、防御力の高い機種を選ぶことが賢明です。
遠心分離機のバイオセーフティ対応とローター選定
細胞の洗浄や回収に使用する遠心分離機は、エアロゾル(微細な飛沫)が発生しやすい工程で使用されます。バイオハザード対策が施された機種を選びましょう。
- バイオシールバケット: 万が一チューブが破損しても、バケット内で菌やウイルスを封じ込められる気密性の高い蓋付きローターが必須です。
- 清掃のしやすさ: チャンバー(回転室)内に結露水が溜まりやすいため、水抜き穴があるか、拭き取りやすい形状かを確認します。
- 加減速設定: 細胞へのダメージを軽減するため、緩やかな加速・減速プロファイルを設定できる機能も重要です。
超低温フリーザー・細胞保存容器の温度管理精度
貴重な細胞マスターバンクや製品を保管する超低温フリーザー(-80℃)や液体窒素容器は、長期的な信頼性が求められます。
- デュアル冷却システム: 2つの独立した冷凍回路を持ち、片方が故障しても-70℃以下を維持できる機種はリスク分散に有効です。
- 温度分布性能: 庫内の場所による温度差が少ないか、バリデーションデータ等で確認しましょう。
- バックアップ: 停電時や故障時に備え、液化炭酸ガス等によるバックアップ冷却装置の取り付けが可能かどうかも確認が必要です。
検体の価値を考えれば、保存機器への投資は保険のようなものです。堅牢性を最優先に選定してください。
顕微鏡・イメージングシステムの記録機能
細胞の形態観察や計数に使用する顕微鏡やイメージングシステムでは、データの客観性と記録性が重視されます。
- デジタル記録: 目視だけでなく、モニターに画像を表示し、デジタルデータとして保存できるシステムが標準的です。
- 記録の真正性: 撮影日時や倍率、操作者情報が画像データと紐付いて改ざんできない形式で保存されるか(DI対応)。
- 操作性: グローブをしたままでも操作しやすいタッチパネルや物理ボタンの配置か。
主観的な判断を排除し、監査証跡として残せる記録機能を持つ機器が、品質保証の観点から望まれます。
環境モニタリングシステムの常時監視能力
CPC内の環境(室圧、温度、湿度、清浄度など)を監視するシステムは、異常を早期に検知するために不可欠です。
- 常時監視と記録: 24時間連続でデータを記録し、トレンド分析が可能なシステム。
- アラート発報: 設定範囲を逸脱した際に、メールや電話で担当者に即座に通知する機能。
- 設置の柔軟性: 配線工事が不要な無線ロガータイプか、安定性の高い有線タイプか、施設の構造に合わせて選択します。
設備単体だけでなく、施設全体の健全性を証明するための統合的な監視体制を構築しましょう。
設備導入プロセスにおける適格性評価(バリデーション)の手順

設備を選定し購入しても、すぐに製造に使用できるわけではありません。GCTP/GMP下では、設備が期待通りの性能を発揮することを検証する「適格性評価(バリデーション)」が必要です。Vモデルと呼ばれる概念に基づき、段階を追って確認を進めていきます。
ユーザー要求仕様書(URS)の策定と明確化
すべての出発点となるのが、ユーザー要求仕様書(URS:User Requirement Specification)の策定です。「どのような設備が必要か」を文書化するプロセスです。
- 使用目的の明確化: 何を製造し、どのような工程で使用するのか。
- 必須要件の定義: 処理能力、サイズ、材質、制御範囲、警報機能など。
- 規制要件の反映: GCTP、DI対応、安全性規格など。
URSが曖昧だと、納入後に「欲しかった機能がない」といったトラブルの原因になります。関係者で十分に議論し、詳細に定義することが成功への第一歩です。
設計時適格性評価(DQ)による仕様確認
設計時適格性評価(DQ:Design Qualification)は、発注しようとしている設備の仕様が、URS(ユーザー要求仕様書)を満たしているかを机上で確認する作業です。
- メーカーから提出された仕様書、図面、カタログなどを照合します。
- 設置場所のユーティリティ(電源、ガス等)と適合しているかもこの段階で最終確認します。
- 不適合があれば、発注前に修正やオプション追加を行います。
DQを確実に実施することで、納入後の「仕様違い」という致命的なミスを防ぐことができます。
据付時適格性評価(IQ)の実施内容
据付時適格性評価(IQ:Installation Qualification)は、機器が現場に搬入された後、正しく設置されたかを確認するプロセスです。
- 現物確認: 発注した型式、付属品が揃っているか。
- 設置状況: 水平に設置されているか、周囲のスペースは確保されているか。
- 接続確認: 電源、ガス、給排水が図面通りに正しく接続されているか。
- 初期設定: 時刻設定や単位設定などが適切に行われているか。
通常はメーカーのエンジニアが実施するケースが多いですが、ユーザー側も立ち会い、記録を確認することが重要です。
運転時適格性評価(OQ)の実施内容
運転時適格性評価(OQ:Operational Qualification)は、機器が仕様通りの範囲で正常に動作するかを確認する試験です。無負荷(検体を入れない状態)で行うのが一般的です。
- 機能確認: スイッチ類、タッチパネル、警報ブザーなどが正常に作動するか。
- 性能確認: 設定温度への到達時間、温度安定性、回転数の精度などが仕様を満たしているか。
- 停電復帰試験: 電源遮断後に設定が保持され、自動復帰するか。
機器単体としての性能が保証されていることを、客観的なデータで証明します。
性能適格性評価(PQ)での実運用確認
性能適格性評価(PQ:Performance Qualification)は、実際の製造に近い条件(負荷状態)で、プロセス全体として期待される性能が得られるかを確認する最終段階です。
- 負荷試験: 実際の検体や模擬検体を入れて培養や遠心を行い、結果が基準内か確認します。
- 連続運転: 一定期間連続稼働させても問題が起きないか検証することもあります。
PQが完了して初めて、その設備は製造に使用可能(リリース)となります。この一連の流れを計画的に進めることが大切です。
設備選定時によくある失敗事例と対策

設備選定には落とし穴が多く、細部を見落とすと導入後に大きなトラブルに発展することがあります。ここでは、実際によくある失敗事例とその対策を紹介します。これらを事前にチェックリストとして活用し、リスクを回避してください。
搬入経路や設置スペースの確認不足によるトラブル
もっとも初歩的かつ頻発するトラブルが「部屋に入らない」という事態です。
- 失敗例: 機器のサイズは確認したが、エレベーターの扉の高さや、廊下の曲がり角、CPC前室のパスルームの寸法を考慮していなかった。
- 対策: 搬入ルート全体の寸法を実測し、養生(保護材)の厚みも含めてシミュレーションを行うこと。必要であれば、機器を分解して搬入し、室内で組み立てる「現地組立」が可能かメーカーに相談しましょう。
図面上の寸法だけでなく、実際の現場を確認することが不可欠です。
ユーティリティ(電源・ガス・給排水)の容量不足
機器を動かすためのインフラ(ユーティリティ)の不整合もよくある問題です。
- 失敗例: 海外製機器を買ったらコンセント形状が違った、電圧(100V/200V)が合わなかった。CO2インキュベーターに必要なガス供給圧力が足りず、アラームが鳴り止まない。排水ピットがなく、オートクレーブが設置できない。
- 対策: URS策定時に施設側の供給能力(一次側)と機器の要求仕様(二次側)を詳細に突き合わせること。特に電源容量は、起動時の突入電流も考慮する必要があります。
海外製品導入時の部品調達とメンテナンスの遅延
海外製の先端機器は魅力的ですが、運用面でのリスクが潜んでいます。
- 失敗例: 故障時に交換部品の取り寄せに数週間かかり、その間製造がストップした。マニュアルが英語のみで、現場スタッフが操作を誤った。
- 対策: 国内代理店のサポート体制(技術員の人数、部品在庫の有無)を厳しくチェックすること。また、日本語の操作マニュアルや簡易手順書の作成を条件に含めるなど、現場での使いやすさを確保する工夫が必要です。
排気・廃液処理設備の法令対応漏れ
設備から出る排気や廃液の処理は、環境法令に関わる重要な問題です。
- 失敗例: 安全キャビネットの排気を室内に戻していたが、取り扱う物質によっては屋外排気が必須だった。感染性廃液を処理するオートクレーブや中和装置の設置を忘れていた。
- 対策: 取り扱う細胞や試薬のリスクグループ、地域の条例(下水道法など)を確認し、適切な処理設備を付帯させること。施設の空調設計担当者とも連携し、排気ダクトの接続可否を事前に協議しましょう。
まとめ

再生医療における設備選定ガイドとして、GCTP適合、バリデーション、そして具体的な機器ごとの選定ポイントを解説してきました。
設備選定は、単なる「モノ選び」ではなく、将来にわたる製造品質と安全性を担保するための「リスク管理プロセス」です。サニタリー性やサポート体制、DI対応といった多角的な視点を持つことで、失敗のリスクは大幅に低減できます。
まずはしっかりとしたユーザー要求仕様書(URS)を作成し、自社に本当に必要な要件を定義することから始めてみてください。適切な設備導入が、貴社の再生医療事業の発展を支える強固な基盤となることを願っております。
設備選定ガイドについてよくある質問

設備選定に関して、現場の担当者様からよくいただく質問をまとめました。導入検討時の参考にしてください。
-
中古の理化学機器を導入してもGCTP上問題ありませんか?
- 不可能ではありませんが、推奨はされません。前の使用履歴(汚染リスク)が不明確な場合が多く、適格性評価(バリデーション)を一から実施するコストを考えると、結果的に新品の方が安定的かつ安価になるケースが多いでしょう。
-
家庭用の冷蔵庫を試薬保管に使っても良いですか?
- 再生医療等製品の製造用としては避けるべきです。家庭用は温度分布の精度が低く、庫内温度のデジタル記録や警報機能がないため、厳格な品質管理が求められるGMP/GCTP要件を満たすことが困難です。
-
ユーザー要求仕様書(URS)は誰が作成すべきですか?
- 基本的には設備を使用するユーザー(製造部門や設備管理部門)が作成します。ただし、専門的なスペック記述が難しい場合は、メーカーやコンサルタントの支援を受けながら、自社の要求を具体化していく方法も一般的です。
-
設備のメンテナンスや校正はどのくらいの頻度で行うべきですか?
- 一般的には1年に1回が目安ですが、機器のリスク評価に基づいて決定します。使用頻度が高い機器や、重要工程(重要パラメータに関わるもの)に使用する機器は、半年ごとの点検が必要な場合もあります。
-
海外製と国産、どちらを選ぶべきでしょうか?
- 一概には言えませんが、最先端の機能や実績を重視するなら海外製、迅速なサポートや部品供給の安定性を重視するなら国産が有利な傾向にあります。両者のメリット・デメリットを比較し、自社の優先順位に合わせて選定しましょう。